 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


[单选]
在一般情况下,只要两电对的电极电位只差超过(),该氧化还原反应就可用于滴定分析
A、E1-E2≥0.30V
B、E1-E2≤0.30V
C、E1-E2≥0.40V
D、E1-E2≤0.40V
 答案
答案
查看答案
 更多“在一般情况下,只要两电对的电极电位只差超过(),该氧化还原反应就可用于滴定分析……”相关的问题
更多“在一般情况下,只要两电对的电极电位只差超过(),该氧化还原反应就可用于滴定分析……”相关的问题
第10题
参照标准电极电位数据,按在酸性溶液中氧化能力增加的顺序将下列物质重新排列。 分析判断氧化能力的大小一般比较不同电对的标准电极电位的相对大小,一般为:氧化型电对中,
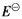 大的是相对强的氧化剂,即氧化能力强。 I2,F2,KMnO4,K2Cr2O7
大的是相对强的氧化剂,即氧化能力强。 I2,F2,KMnO4,K2Cr2O7
请帮忙给出正确答案和分析,谢谢!
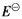 大的是相对强的氧化剂,即氧化能力强。 I2,F2,KMnO4,K2Cr2O7
大的是相对强的氧化剂,即氧化能力强。 I2,F2,KMnO4,K2Cr2O7请帮忙给出正确答案和分析,谢谢!
第11题
已知E0Hg22+/Hg=0.793v和Hg2Cl2的ksp=1.3×10-18若在Cl-保持0.010mol/L溶液中则上述电对的电极电位应是()
A、0.026V
B、-0.026V
C、0.383V
D、-0.383V








 大学生认证
大学生认证





