 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


根据SO2通入不同溶液中的实验现象,所得结论不正确的是()
A、通入含HCl、BaCl2的FeCl3溶液,产生白色沉淀,说明SO2有还原性
B、通入H2S溶液,产生黄色沉淀,说明SO2有氧化性
C、通入酸性KMnO4溶液,紫色溶液褪色,说明SO2有漂白性
D、NaHCO3溶液,产生大量无色无味气体,说明酸性:H2SO3>H2CO3
 答案
答案
 更多“根据SO2通入不同溶液中的实验现象,所得结论不正确的是()……”相关的问题
更多“根据SO2通入不同溶液中的实验现象,所得结论不正确的是()……”相关的问题
第3题
①向饱和碳酸钠溶液中通入过量CO2②向Fe(OH)3胶体中逐滴滴入过量的H2SO4
③向Ba(NO3)2溶液中通入过量SO2④向石灰水中通入过量CO2
⑤向硅酸钠溶液中滴入过量的盐酸.
A、①②③
B、①②⑤
C、①②③⑤
D、①③⑤
第6题
A、将二氧化碳通入紫色石蕊溶液中:紫色石蕊溶液变蓝色
B、高锰酸钾放入汽油中:很快溶解形成紫色溶液
C、氢氧化钠固体放置于空气中:表面潮湿并逐渐溶解
D、涤纶和羊毛燃烧:都可闻到一股烧毛发的焦糊味
第7题
A、除去H2中混有的少量HC1:通入盛有氢氧化钠溶液的洗气瓶,干燥
B、检验NaOH溶液是否变质:加入几滴无色酚酞试液,观察现象
C、鉴别NaOH固体和NH4NO3固体:加水溶解,观测溶液温度变化
D、除去NaCl中混有的少量Na2CO3:加入过量氯化钡溶液,过滤,蒸发结晶
第8题
A、选项实验操作实验现象实验结论
B、A甲苯和酸性高锰酸钾溶液混合紫色退去甲苯分子中含碳碳双键
C、B乙醇与浓硫酸共热170℃所得产物直接通入酸性高锰酸钾溶液紫色退去有乙烯生成
D、C乙醇在铜做催化剂时被氧气氧化,产物与新制氢氧化铜共热看到红色沉淀产生有乙醛生成
E、D某物质和银氨溶液反应有银镜生成该物质一定是醛
第9题
羟胺又称为胲,是无色,无嗅,易潮解的晶体,熔点为330C,加热容易爆炸。羟胺具有弱碱性,可以和硫酸,盐酸等强酸形成盐。羟胺及其盐是重要的有机合成中间体,在有机合成中用于合成肟,多种药物,己内酰胺等。以下是合成羟胺的一种方法:
在00C时,将SO2缓慢通入亚硝酸钠和亚硫酸氢钠的混合溶液(三者摩尔比1:1:1)中,得到一种负二价阴离子A,A完全水解得到羟胺的硫酸盐溶液,所得溶液为强酸性。已知A中氮元素质量分数为7.33%,含N-O、N-S、S-O等四种类型的化学键。
1画出A以及羟胺的硫酸盐的结构式。
2写出合成羟胺的反应方程式。
3一定条件下羟胺可以与卤代烃(RX)反应生成两种不同类型的化合物,写出合成反应方程式,指出反应的类型。
4纯羟胺可以用液氨处理羟胺的硫酸盐得到,写出反应方程式,并说明如何除去杂质。
5纯羟胺在空气中受热容易爆炸,写出爆炸反应方程式。
第10题
A,B,C,D,E,F是分属三个短周期的主族元素,且原子序数依次增大。A,D同主族,B的简单气态氢化物的水溶液呈碱性,E,C同主族,形成的化合物EC2是形成酸雨的主要物质之一。请回答下列问题:
(1)F在元素周期表中的位置为()。
(2)D2E溶液在空气中长期放置会发生反应,生成物之一为H。H与Na2O2的结构和化学性质相似,其溶液显黄色。写出D2E溶液在空气中长期放置生成的化学方程式:()。H溶液与稀硫酸反应产生的现象为()。
(3)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为()。
(4)向30mL某浓度由A,B,C,D中的三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向溶液M中逐滴加入0.1molL盐酸,产生的气体体积【V(CO2)】与加入盐酸的体积【V(盐酸)】的关系有如图所示两种情况(不计CO2的溶解)。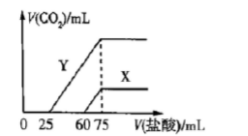 ①原一元强碱溶液的物质的量浓度为()MOL/L。
①原一元强碱溶液的物质的量浓度为()MOL/L。
②由曲线X,Y可知,两次实验通入的CO2体积之比为()。
第11题
A、酸性KMnO4溶液中通入SO2气体后紫色消失
B、显红色的酚酞溶液通入SO2气体后红色消失
C、SO2通入品红溶液气体后红色消失
D、溴水通入SO2气体后橙色消失
请帮忙给出正确答案和分析,谢谢!








 大学生认证
大学生认证





