 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温同体积同浓度的HCN和HClO说法正确的是()
A、电离程度:HCN>HClO
B、pH:HClO>HCN
C、与NaOH溶液恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D、酸根离子浓度:c(CN-)<c(ClO-)
 答案
答案
 更多“相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温同体积同浓度的HCN和HClO说法正确的是()……”相关的问题
更多“相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温同体积同浓度的HCN和HClO说法正确的是()……”相关的问题
第1题
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备路线如下: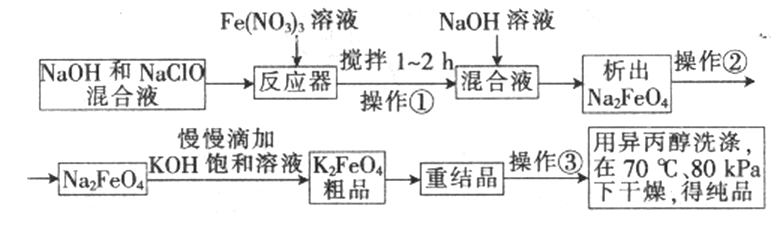
试答复以下问题:
问题一、操作①搅拌的目的是:()。
问题二、操作②与操作③相同,该操作名称是:()。
问题三、反应器中,NaOH、NaClO及Fe(NO3)3反应的离子方程式为:()。
问题四、次氯酸钠浓度对高铁酸钾产率有一定影响,当高铁酸钾产率最高时,NaClO的物质的量浓度约为()。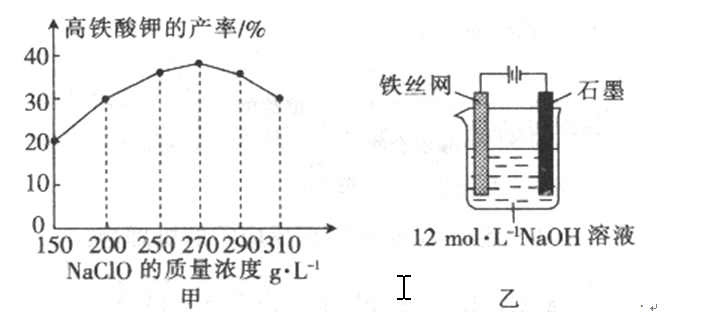
问题五、从环境保护的角度看,制备中间产物Na2FeO4较好的方法为电化学法,其装置如图乙所示,则阳极的电极反应式为()。
第3题
原料的数量和浓度相同,用简单蒸馏得汽相总组成为xD1,用平衡蒸馏得汽相总组成为xD2。若两种蒸馏方所得的汽相量相同,则:()。
A、xD1>xD2
B、 xD1=xD2
C、
xD1 D、不能判断
第10题
A、①②③⑤
B、①②④⑤
C、②③⑥
D、②④⑤
第11题
A、NaHCO3固体受热容易分解,而Na2CO3固体受热不容易分解
B、等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者消耗盐酸的物质的量比后者多
C、等物质的量浓度的Na2CO3和NaHCO3溶液分别滴加2滴酚酞试液,前者颜色比后者深
D、Na2CO3溶液和NaHCO3溶液分别与Ba(OH)2溶液反应的离子方程式相同








 大学生认证
大学生认证





