 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是()
A、达到化学平衡时,4v正(O2) =5v逆(NO)
B、若单位时间内生成n mol NO的同时,消耗n mol NH3,则反应达到平衡状态
C、达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D、化学反应速率关系是:2v正(NH3) =3v正(H2O)
 答案
答案
 更多“对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是()……”相关的问题
更多“对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是()……”相关的问题
第1题
A、若单位时间内生成xmol NO的同时,消耗xmol NH3,则反应达到平衡状态
B、达到化学平衡时,若增大容器的体积,正反应速率减小,逆反应速率增大
C、达到化学平衡时,若升高温度,正反应速率增大,逆反应速率也增大
D、化学反应反应速率关系2υ正(NH3) = 3υ正(H2O)
第2题
A、v(NH3)=0.01 mol·L−1·s−1
B、v(O2)=0.001 mol·L−1·s−1
C、v(NO)=0.001 mol·L−1·s−1
D、v(H2O)=0.045 mol·L−1·s−1
第3题
A、0.01mol/(L·min)
B、0.6mol/(L·min)
C、0.06mol/(L·s)
D、0.12mol/(L·min)
第4题
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
问题一、选择性催化复原法的脱硝原理为:

①上述反应中每转移3mol电子,生成标准状况下N2的体积为()L。
②已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ•mol-1
N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ•mol-1
N2(g)+O2(g)=2NO(g)ΔH=-180.5kJ•mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH=()。
问题二、目前,科学家正在研究一种以乙烯作为复原剂的脱硝(NO)原理,其脱硝机理示意图如以下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。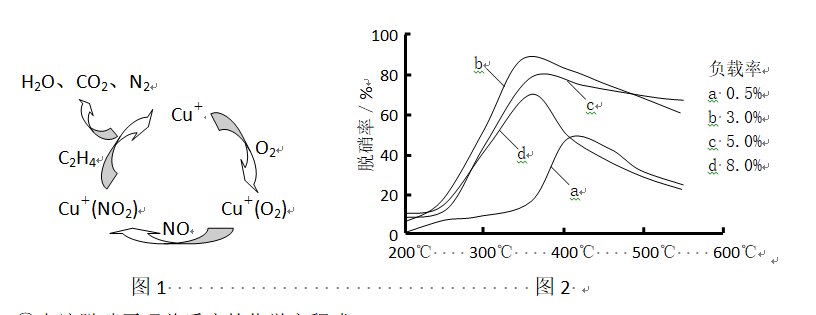
①出该脱硝原理总反应的化学方程式:()。
②为到达最正确脱硝效果,应采取的条件是()。
第6题
A、增大压力
B、增大D的浓度
C、使用催化剂
D、升高温度
第7题
A、M、N全部变成了P
B、反应已经停止
C、反应混合物中各组分的浓度不再改变
D、v(M)∶v(N)=2∶1
第8题
A、生成1molCO的同时生成1molH2
B、容器中物质的总质量不发生变化
C、n(H2O):n(H2)=1 :1
D、v逆(H2O)=v正(CO)
第9题
A、(N2)∶c(H2)∶c(NH3)=1∶3∶2
B、氨气的百分含量不再变化
C、断开1个N≡N键的同时有6个N—H键生成
D、混合气体的质量不随时间的变化而变化
第10题
A、体系的压强不再发生变化
B、v正(CO)=v逆(H2O)
C、生成n mol CO的同时生成n mol H2
D、1 mol H—H键断裂的同时断裂2 mol H—O键
第11题
A、③、④、⑤、⑥
B、②、③、④、⑥
C、①、③、④、⑤
D、①、③、④、⑥








 大学生认证
大学生认证





